物理科学探疑-物质的存在-球壳式原子核结构模型―和原子核外电子的力学分布方法
![]()
球壳式原子核结构模型
――――和原子核外电子的力学分布方法
志勰
采用力学的模式对原子核所建的一种全新的理论模式。该理论认为原子核是一种中空的球体,质子和中子分布在球体的表层上。对于前10号元素,该理论可以合理的推出稳定原子核的质量数,并且和常规的吻合。对核理论模型、核结构、核聚变、研究前10号元素的原子核有参考价值。(该文修正了17O(2)、18O(2)错误的问题,时间2002.9.22)
一、引言
1911年,英国卢瑟福采用a粒子散射实验证明了原子的大部分质量集中在原子中心,并且这个原子中心带有正电荷之后,一个不争事实就确立了。原子是由原子核构成,并且带有正电荷,原子核外存在带负电的电子。在这个基础上,卢瑟福提出原子的有核结构。1919年,卢瑟福在用a粒子轰击氮原子核的试验的时候,确定了质子的存在。1932年,英国物理学家查德维克在研究博特和贝克尔发现的穿透力很强的射线中确定了中子的存在。这样原子核是由质子和中子构成则被人们所公认,并拉开了揭示原子核结构的序幕。
二、传统的原子核模型
最早被人们提出的原子核模型是气体模型,这种模型认为原子核中的质子、中子是类似于气体分子的集合,但由于该模型说明原子核的性质不多,而被人们所淘汰。
第二种模型为液滴式模型,是在二十世纪三十年代由丹麦的玻尔等提出,主要利用核力的短程、饱和性质,把原子核看成一个密度很大的液滴,对核裂变、原子核的稳定性、推算原子核的半经验质量公式获得了很大的成功,但对原子核的细节上的描述,很难做出有效的说明。
第三种模型是a粒子模型,主要依据是原子核a粒子衰变以及一些原子核具有整倍数的a离子的特征,但大量的事实不支持这样结论。
第四种是壳式模型,对原子核的试验结果进行归纳的结果,核子的递加所呈现的特定的规律性,比如当质子和中子的数目等于2、8、20、28、50、82、126时,原子核特别稳定、结合能特别大。就成这些数为幻数。这些现象显示,原子核内部的填充可以和原子内部的填充相类似,存在某种壳层结构。根据这一模型,当原子核中的质子和中子的数目为幻数时,核子恰好填满封闭的壳层。壳层模型是采用量子论的方法在粒子独立运动的基础上提出的,不能体现核子间的相互作用。
第五种是综合模型,壳层模型注重于单个的核子运动的研究,液滴模型则把原子核所有的运动归结为整个集体的运动,把这两种模型综合起来考虑就是这种综合模型。
对如上五种原子核模型,从力学的角度上我不认为是合理的。因为最重要的是在如上五种模型中没有处理作为物理基础的因果关系,也就是力学的依据。第一种模型原子核没有使原子核中的各个核子凝聚在一起的作用,必然会不存在。第二种模型因为短程核力的作用,必然会最终形成稳定的固体的结构。第三种模型原子核的质量上是不遵守这样的规律的。第四种模型,如果核子间存在着相互作用,那么这些核子又怎么能在稳定的轨道上运行呢?这显然是很难的。即便采用综合的方法来提出第五种的综合模型,那么这又怎么能合理的解释呢?
三、组建原子核的可能模式
原子核是由带正电的质子和不带电荷的中子组成,这样的在试验的基础上的事实是不需要争辩的。那么我们对于原子核的模型就已经有了组建的材料,那就是质子和中子。我们只能在这个基础上来讨论原子核的结构。
中子是不带电的,通常我们把中子看作是粘合质子的物质粒子,来进而保证原子核的稳定性。关于中子的属性,在文中还要探讨。
原子核的体积是非常的小,(现在人们的看法为原子核的形状接近球型,其半径R和质量数A存在R=r0A1/3,其中r0为一常数,精密测定为1.20×10-15m。)([简明物理手册]上海辞书出版社出版1987年12月第一版)。如果质子在这样小的空间里存在相互作用,那么我们只要根据库仑定律粗略估算一下,两个质子间的作用力的大小为1.97×10-2牛顿。试问这样大的作用力作用在质子身上它又怎么能在各自的轨道上不受任何影响的自由的运动呢?很显然,在这样强大的作用力的作用下,质子不可能存在什么运动。即便是考虑上强相互作用和弱相互作用。那么,从力学的角度上,质子必然处于一种作用力的平衡状态。如果我们仍然采用中子是粘合质子的粒子,那么原子核的模型则只有一种了,那就是球壳式原子模型。我们先来看这样一种现象:
我们将园气球吹上气,那么气球则会呈现圆形。肥皂泡在没有空气流动的空间中,它必然也是标准的球形。给一块金属施加电荷,电荷会分布在金属的表面。前者,是空气分子给与气球壁或者肥皂泡膜均匀的作用力,气球壁或者肥皂泡膜在自身张力的作用下会呈现球形。后者,是电荷本身的作用,使电荷均匀的分布在金属表面,中空薄膜在内力均匀作用下的自由分布的则必然是球形。
原子核也具有这样的特征,质子之间存在的强大的作用力,在中子粘合的作用下,必然是一种中空的球形。并且稳定原子核的质子和中子是静止的。从力学上来说,这是质子和中子构成的原子核的模型的一种最具可能的方式。
这样一种原子核模型我想大家都感到意外,在一个球上,带正电的质子趋向于分布在球皮上,就像乒乓球一样,球心是空的。
下面,我们来探讨原子核中核子间力学作用的结构特征。
四、核子间的作用规律
1、原子核给与核子的作用特征
(1)中子对质子的粘合特征
第一、中子对质子粘合特征的存在
从原子核的组成上,我们将构成原子核的粒子当作两种不同种类的粒子,前面我们也说了这个问题,就是质子和中子是构成原子核的两种基本材料。那么具有质子和中子应该具有什么样的特征呢?
中子是质子的粘合粒子这一点在客观事实上是确定的。因为我们不能找到没有中子粘合的多质子原子核。如果原子核含有两个质子以上,那么在原子核中至少存在存在一个中子。在现在来说,这是客观事实。
第二、中子对质子粘合特征的意义――强相互作用
中子和质子之间存在粘合特征说明质子和中子之间存在一种确定的相互作用,至于这种相互作用的性质,在传统物理学中,通常将这种相互作用叫做强相互作用。被认为是将核子束缚在一起的作用力,其作用程在原子核线度的范围,即10-15米。当然,这是传统的看法。
第三、强相互作用的数量级的不合理性
关于强相互作用的范围,我认为这样的判断是不合理的。我们不能根据原子核的大小来判断强相互作用的范围,因为虽然在原子核中包含这种强相互作用,但并没有足够的证据说明强相互作用源发出的每一个强相互作用必然的作用于整个的原子核。
如果强相互作用源来自于质子和中子之间,那么强相互作用距离必然远小于10-15米,其距离原子核中质子和中子之间的质心的距离,我们知道,强相互作用不会超过2倍的这个距离,如果要远大于这个距离,那么在解释和反应时,就会容易出现问题。当然,这仅仅是一种假设,为了探讨束搏质子之间的这种作用,那么我们首先来看一下质子之间的作用。
(2)原子核中质子、中子对外界的作用
由于质子携带一个单位的正电荷,那么它表现为电的作用。在原子的范围,库仑定律是不能严格成立的。(可参见本站电磁理论与原子论栏目中的电磁理论与原子论之一库仑定律的适用范围)这说明,电的属性的作用在原子核的范围是不能成立的,但是,质子和中子是可以作为点源粒子来看待的,那么它就应该遵守点源粒子对外作用的特征。那么我们可以先看看,点源粒子作用的特征。
在电荷的属性――以及基本电荷相互作用的特点,我们已经探讨了点源粒子作用的特点,质子也是一种点源粒子,它也具有点源粒子作用的这样的两个哲学观念。即:
一个观念是作用源对外界提供的作用不会因为在空间的延伸而在它提供的总的作用数量上而减弱。
另一个观念是在不存在其它作用的时候,空间的任意点作为作用的载体是各向同性。
(可参见时间空间与物质的运动栏目中的电荷的属性――以及基本电荷相互作用的特点)
在原子核中,粒子间的距离非常短,这样的点源作用是抽象的,我们不能采用任何的方法来直接得到核子间的作用规律,而只能对原子核中核子间的可能性的结构进行判断。在某种意义上来说,存在非常大的不确定度。换句话说,我们判断的结果未必是真实的核子间作用。但是,我们不能找到拒绝点源粒子作用的两个哲学观念的理由。如果我们要拒绝这样的两个观念,那么必须具有这样的条件:
第一、质子和中子不是基本的粒子,具有内在的结构,并且这种结构是非中心对称体。
第二、质子和中子是基本的粒子,但是它本身对外作用的分布,不具有中心对称结构。或者换句话说,质子和中子的粒子表面对外界的作用分布不是均匀的。
在如上两个特点中,质子和中子存在的磁矩对此有违背作用,磁矩的存在似乎说明质子和中子是左右对称的分布结构,而不是中心对称。但是,我们没有任何的理由认为质子和中子是左右对称的(或者轴对称)。这样的结论主要基于如下两点原因:
第一、中子在932秒后,通过β衰变释放出反中微子和电子转化为质子,如果质子、反中微子、和电子是构成中子的,那么从可能性的结构上来说,它不可能是中心对称,也不可能是左右对称。
另一方面,中心对称和左右对称都是稳定的分布形式,具有中心对称和左右对称的粒子,应该是稳定的作用结构。在后面核子排布分布规律中有一个结论,属于中心对称的原子核是稳定的原子核,中心对称的在氢原子中也具有稳定的特性,但是在重原子核中则是较为稳定的了。
第二、质子是稳定的,到目前为止,还没有发现质子的衰变。那么,在目前我们完全可以认为质子是一种基本粒子,那么稳定的中心对称体则是一种必然。
因此左右对称不适合应用于中子和质子,至于磁矩应该采用其它的模式进行处理。对于质子、中子采用什么样的作用模式,可以确定的是质子必然是符合中心对称体的模式。质子可以采用点源作用模式进行处理。
对于中子还不能确定,但可以确定的一件事就是,中子之间存在一种斥力(可参见氢原子核)。我们在原子核的结构中也要考察这个问题。对于中子可以采用的作用模式,在后面有结论。
2、原子核的大小
(1)经典的原子核的大小
原子核的大小通常被看作是采用试验验证的,通过a粒子库伦散射实验来完成的。比如原始的方法,卢瑟福采用a粒子轰击铝箔的方法。原子核半径R和质量数A存在R=r0A1/3便是这样的结论。那么采用这样的方法是不是有效呢?
在传统的测定原子核大小的方案中(可参见任意一本含有原子核内容的大学物理学),包含有两个假设,分别为:
第一、原子核的体积V近似于质量数成正比
![]()
第二、原子核的密度为
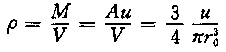
其中u、r0都是常量。这和原子核的模型是不无关系的。我认为这样的假设其依据是不够的。我们有什么理由确定这两个假设为真呢?采用本文提出的球壳式原子核结构模型当然不能采用这样的方法。不能将原子核的体积看作近似于质量数成正比,也不能将原子核的密度当作均匀看待。下面我们就来探讨这个问题。
(2)轻原子核大小的计算方法
在质子数量较少的情况下,质子数在原子球壳不能完成一个中心对称球体分布的情况下,因为力学平衡状态是唯一的,那么质子和中子在原子核中的分布都存在确定的结构。当然,这并不是说相同种类和数量的核子所构成的原子核是唯一的,它可以构成不同结构核子分布的原子核,但必须满足力学平衡状态。一种原子核核子的分布仅对应一种核子力学平衡状态结构。比如5锂就存在两种可能的分布。如图:
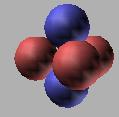

红色的球表示的是质子,蓝色的球表示的是中子。但第二种排成直线形状的没有第一种原子核稳定,在碰撞中比较容易分裂成四个质量的氦原子或者两个质量的氢原子。
对于轻原子核,只能根据具体的核模型进行具体的计算核结构、大小。
(3)原子核大小的计算方法
对质子数较多的原子核和重原子核,则存在一种简单的结算方法。根据球壳式原子模型,所有的质子都均匀的分布在一个球层上(根据力学原理,所有的原子核都是趋近于这种模式),那么只要确定了质子和中子的大小及作用距离,就可以近似的计算这种原子核的大小。在球壳式原子模型中,计算原子核的密度是没有意义的,因为球壳的中心是空的,没有其它的粒子。但可以计算平均密度。相同质子数的原子核的密度必然是不同的。
为了便于简化计算,我们仅计算由质子构成的球壳就行了。由于质子和中子的质量相差不大,那么可以将中子和质子的直径近似看作是相等的。这就提供给我们一种简单粗略的计算方法。仅适用于稳定核的计算。我们可以分以下几种来计算原子核的大小:
第一种,中子数等于或者小于质子数。中子数小于质子数的原子核,只存在于质子数较小的原子核中。可以采用球面积公式来计算。如下
![]()
其中,S=2nr2,为球面积,n为质子的个数,r为质子的直径,r2表示一个质子所占据的球壳表面积。R为核半径。我们可以根据这个关系来近似的求出原子核的半径。
第二种,中子数大于质子数但小于或者等于2倍的质子数。
原子核的半径大于R小于R+(1/2)r
第三种,中子数大于2倍的质子数。
原子核的最大半径为R+r。
3、原子核的结构方法
(1)力学结构
如果我们将原子核的组分看成是由中子和质子构成,那么质子间由于存在的相互斥力,必然存在一种张力。这种张力使中子作为一种粘合力,首先使中子充当于质子之间克服斥力的连线。
质子之间的张力有两种模式的力构成,一种模式是相邻两个质子之间的斥力,另一种模式一个质子和非相邻的质子之间的斥力。
当质子的数量非常的多时,那么质子之间的斥力将会增加。当一个中子连接两个质子之间的作用力小于质子之间所构成的张力时,那么原子核如果要稳定,那么必然要增加中子对质子的粘合力。如图:
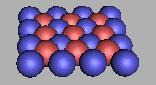
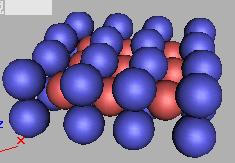
图中左图的小图片是普通原子球壳的一部分,右图的大图片是理想化重原子核球壳的一部分,但不是真正的原子球壳,仅仅是为了说明这个问题而画的说明性的东西。因此,普通原子球壳质子和中子之间的作用数量关系可以看作是1:1作为稳定的模式,对于重原子核则是1:2了。在实际的原子核结构中,稳定的原子核其中子数大于两倍的质子数小于三倍的质子数。轻原子核则例外。因此,质子和中子的作用实际上是存在这种限制的,质子和中子只能按一定范围在原子球壳上进行排布,这一点是由于质子和中子之间的结构模式所决定的。
(2)原子核中质子数的极限
当质子数和中子数的结合不能满足于稳定的结构时,即:质子之间的张力大于中子之间的粘合力的时候,那么这种情况下,质子数则不能再递增。不论如何排布中子,都不能完成中子对质子的粘合力大于或者等于质子之间的张力,那么这也是原子核中质子数的最大值。也就是说,原子核的质子数存在一个上限。理论上可以计算出来,这需要很好的数学以及对原子核更为详尽的分析。因为中子和质子之间、中子和中子之间的作用并不能确定。
(3)填充方法和原子核的性质
在质子数为确定值后,相同质子数的原子核,存在多种。因此适当的增加中子数量可以得到不同的同位素。在一个稳定的核上增加中子,是一种构造同位素的方法,在这里,我把它叫做中子填充法。利用该种方法,可以构造出所有的原子核。
填充中子需要在稳定或者较为稳定的原子核上进行,否则,填充中子会造成原子核的分解。
在填充中子的过程中,应遵守最大作用原则。首先填充到对中子最大作用的核位置上。这样核会具有较好的稳定性,当然,也可以填充到不稳定的位置。
在一个稳定核上填充中子的,可以允许多种填充位置,因为在核反应或者和外界作用时(比如a粒子、质子、中子、轻核等)作用时,是随机的。但是每一个填充位置的稳定性决定该新原子核是否具有稳定性。它代表着中子和原子核不同的作用属性。如果所填充的中子使新的核具有放射性,那么不同的填充位置、不同的核原子核的作用属性导致放射的能量是不同的。
在本文中不会将组成所有的可能性原子核的都列出来,只列出最大可能性的填充或者随机一种的填充。比如在11B稳定核的基础上添加一个中子,可以存在9种位置,而我在这里仅采用一种。而填充后在12B的基础上存在8种,也仅列出一种。因为那样的话,所作的图片也就太多了。不同位置的添加会造成不同的原子核的属性,这一点是需要注意的。我在本文中就简化了,有兴趣的可以在3dmax源文件中自己去添加研究。
此外,对可能性较小的结构不再列出来,比如硼的四质子环结构、碳的五质子环六质子环结构等。
关于质子环,在球壳式原子核模型中,在轻原子核到普通原子核的过渡中,由简单的几个质子到球壳原子核模型的过渡过程中,质子数量所构成的圆环的模式。几个质子构成的环就叫做几质子环。我是这样定义的。
(4)中子之间存在斥力
中子之间存在斥力,这是对轻原子核排布的过程中所得出的结论。在原子核的范围,由于库仑定律在表示质子作用的大小和方向上,可能失效。因此,中子之间的斥力还是一个未知的问题。但可以肯定,相同的距离,一个中子和一个中子之间的斥力,要小于一个质子和质子之间的斥力。否则,根据《核素常用数据表》不能排布出和客观事实吻合的核结构。
4、核子间结构的变动――能量的辐射
在原子核由于外来的因素或者内部的不稳定因素,核子间的位置发生变动的同时,原子核要发射高能电磁辐射。其辐射的发射来源于变速运动的质子。
因此,在一个核反应中,有多少个质子的变速运动,就会发射多少次高能电磁辐射。
五、原子核外电子的力学分布方法
在原子核的核子结构的排布确定之后,那么确定原子核外电子的力学分布则成为一种较为简单的事情了。只需要按照核外电子在原子核外所受到的作用力的大小来排布就可以了。
只具有几个质子数的原子核,核外电子的排布是要容易一些,但是对于拥有几十个质子的原子核来说,则远非这样简单。那么,这就需要建立一种方法来简化力学排布所需要的大量的计算。那么,采用什么样的方法才可以简化和确定呢?
如果原子核的质子在原子核球壳上的分布唯一的确定,那么最内层的电子和质子间的作用也是唯一确定的。这样就确定了原子核外最内层电子的分布。
电子之间存在斥力,这是一个不争的事实。那么距原子核第二层电子如何排布,根据力学的方法则可以确定。电子即受到原子核中质子的引力作用,同时也受到距原子核第一层电子的斥力作用,电子所受到的作用力最小的空间位置就是距原子核第二层电子在核外空间所分布的位置。距原子核第三层电子在核外空间的分布也是同样的。
这样,原子核外电子在核外空间的分布就唯一的确定了。这样,在没有外来作用的情况下,静止的核模型就可以这样确立了。
由于不同元素原子核内的质子在球壳上的分布是不同的,即便是相同元素不同的原子核,质子的分布也未必是相同的,那么不同元素核外电子在核外空间的分布也是绝然不同的。考虑到中子的存在并可能影响核外电子的分布,因此,核外电子的分布仍然是非常复杂的。本文提出的方法是忽略掉中子对核外电子的影响,并作为异种简化处理的方法。
六、轻原子原子核结构规律和轻原子核图谱
1、氢原子核 3D源文件
(一)原子核属性
氢原子核可能存在的结构为1H、2H、3H、4H、5H。氢原子核只具有一个质子,已经发现的氢原子核有氢、氕、氘三种原子核。如图:
|
|
|
|
|
图中红色的球代表质子,蓝色的代表中子。后两种氢原子核是根据力学的稳定性来判断应该存在的可能性结构。前三种我就不用说了,想必大家都知道。后两种分别是4H和5H。4H质子和中子都处于一个平面,其中中子和质子的相邻连线成120度的角度。5H中四个中子构成正四面体,质子位于中间。
后两种到现在为止还没有被发现,我想是主要是在自然界中和常规的核反应中不易生成。存在时间极短。其中5H已经达到力学的饱和状态。因此不会再存在比5H质量还要大的氢原子核。另一方面,采用排列和组合的方式,4H是有可能被发现的原子核。氘的半衰期为12.33年,只要采用适当速度的中子去照射氘,那么有可能形成4H。
5H是不能被证明的,在目前来判断,自然界中没有核反应或者通过可能的方式来满足实现这样的核结构。当然,如果4H半衰期存在的时间较长,那么5H则有可能被发现。
从H原子核来看,中子之间必然存在一种斥力。否则,4H和5H会很轻易的被人们发现。至于为什么会判断存在4H和5H,这是对下几种原子核进行排布时发现的,因为一个质子和三个中子结合、四个中子结合是很平常的事情,在重原子核中,甚至还会存在一个质子和五个中子结合的可能。
这是一个根据客观事实而得出的一个假设。
(二)原子核所形成的化学属性
1H原子核仅包含一个质子,其核外为一个电子,如图:
|
|
1H核外具有一个电子,那么在对外界的作用上,总是表现为一种矢量作用。如果氢原子核外空间一个点源是正电场或者负电场,氢原子都会受到一种作用力,并且氢原子中质子和电子之间的连线就是电场的方向。氢原子得到一个电子便会形成氢原子对外界作用的稳定结构,如图: |
H-在得到一个电子后,将不容易在失去电子或者得到电子,因为作为整个的离子而言,有一个稳定的作用中心,是以质子为中心对称的,但由于携带一个负电荷。会容易受到外界的作用。
两个氢原子容易结合成一个稳定的氢分子,如图:
对氢分子外界某一点的作用力近乎为零。因此氢分子是比较稳定的。
2、氦原子核3D源文件
(一)原子核属性
氦原子核具有两个质子,这是它的特征。可能存在的氦原子核分别为3He、4He、5He、6He、7He、8He,如图:
|
|
|
|
|
|
|
|
||
在氦原子核中,除了7He还没有被发现之外,其它的都已经被发现了。此外,5He存在同核异构体,5He(1)和5He(2)。7He由于中间是三个中子,两端各存在一个中子,因此将是He里最不稳定的原子核。
在氦原子核中,已经出现了一个质子和四个中子的结合。其中,8He已经达到了核子作用的力学饱和,因此,不会在存在比8He质量还要大的原子核。
(二)原子核所形成的化学属性
在氦原子核中,4He是最为稳定的原子核了。我们这里就以4He来分析氦原子的化学属性,如图:
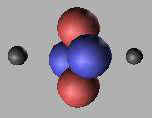 |
4He原子核和核外电子存在电场的作用,那么原子对外界的作用,包括化学反应采用作用力的方法来分析,主要就依赖于电子的电场和质子的电场在空间中的分布所引起的核外界的作用结果。 He原子的质子和电子在一个平面上,这是采用电场作用得到的结果。那么我们采用这四个电荷对原子外层空间一点进行力学的计算,那么该点所受到的作用力为近似为零。 |
因此,4He原子不容易得到电子,同时,由于一个电子都是和两个质子在发生稳定的作用,因此,它也不容易失去电子。因此,它表现为惰性。
另:该气体的组分一定是He原子,而不是由多个原子组成的分子。
3、锂原子核3D源文件
(一)原子核属性
锂原子核具有三个质子,这是它的特征。可能存在的氦原子核分别为4Li、5Li、6Li、7Li、8Li,9Li、10Li、11Li如图:
|
|
|
|
|
|
|
|
|
|
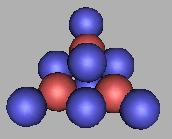 11Li |
其中5Li、6Li、7Li都存在同核异构体。4Li、10Li还没有被发现。6Li(1)、7Li(1)、7Li(2)、8Li是稳定的。其中,8Li和《核素常用数据表》的数据有出入,《核素常用数据表》所测定的8Li是不稳定的。也许传统所测定8Li的不是本文8Li这个原子核。每两个质子之间填充一个中子是可以的,允许得到不同的原子核结构。
4Li是可以被观测到的。可以采用确定速度的质子(原为中子。修改时间2003.3.28)打击3He。其中质子(原为中子。修改时间2003.3.28)的动能要略大于3He原子核的势能。这样可以形成4Li。4Li应该是不稳定的。
(二)原子核所形成的化学属性
7Li(1)是稳定的,我们就以它来分析Li原子的化学属性。质子位于一个平面上,如图: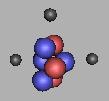
Li原子延三个质子中心轴上相等的距离,各分布一个电子,这两个电子是稳定的。然后在垂直于三个质子中心轴,并且在轴心和两个质子中心的连线上,分布着另一个电子。该电子在没有外界作用的情况下,是稳定的存在。但是当外界对这个电子存在作用并大于这个电子在该区与稳定作用力的时候,这个电子则会在轴心和两个质子中心连线上进行区域的变换,从一个区域移动到另一个区域。该电子由于和三个质子在一个平面上,并且两个电子会对它产生斥力作用,因此这个电子也容易失去。电子所存在的位置和移动所需要的作用,可根据质子和电子的作用进行计算。
由于三个质子成一个平面,并且其中心轴上只存在一个电子,垂直三质子轴心连线的电子,所产生的电场力,对于整个原子来说,不是一种平衡的作用力,因此Li三个质子会对原子外界的电子极易产生电场的引力作用。因此,锂原子极为活泼。
4、铍原子核 3D源文件
(一)原子核属性
铍原子核具有四个质子,可能存在的铍原子核为5Be、6Be、7Be、8Be、9Be、10Be、11Be、12Be、13Be、14Be。
|
|
|
|
|
|
5Be 、13Be没有被发现。其中5Be是不能被发现的,没有生成它的途径。因为它不能从核聚变和核裂变中得到,采用质子轰击也是不可能的,因为4Li可能是不稳定的。
5Be是中子数最少的Be核,它和5H一样难以证实。采用质子轰击4Li的方法很难得到。速度是一个难度很大的问题。速度大了,会引起4Li的分解,速度小了达不到轰击的目的,只有当质子的动能等于4Li的原子核势能时,才可能形成。
7Be(1)不是稳定的排布结构,它最终会通过放射高能电磁射线向7Be(2)过渡。
其中,8Be是最稳定的原子核。这一点和资料中的数据是不同的。《核素常用数据表》中认为8Be是不稳定的,半衰期只有2×10-16秒,而在这里的排布结构中,则是最稳定的。在这种力的结构中,是很难以置信的。我想如果《核素常用数据表》都是通过试验测定的,那么在对8Be的测量中会不会存在问题。在8Be核子的排布结构中,没有其它的可能性。8Be在Be元素中应该是最为稳定的原子核。
在Be元素中,质量大于8Be的原子核的结构排布则出现分歧了,有两种排布思路的可能性。一种可能性是采用中子所受到的作用力最小,那么在8Be外围游荡的中子则容易和8Be外层的质子粘合。这一条是在假设中子之间存在斥力为出发点。但是这条排布方法只能使Be排布到12Be。即:在每一个质子的顶端增加一个中子,这样,Be可以从8Be之后增加四个原子核,所增加的这四个原子核,从力学结构上来说,应该都是较为稳定的。如图:
|
|
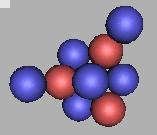 11Be(1) |
|
另一条排布思路是中子所受到的质子的粘合力最大的原则,当8Be原子核受到能量较高的中子轰击时,则容易按这条思路进行排布,并且可以使Be排布到质量数为14。每一核外每两个质子的夹隙,都可以填补一个中子。如图:
|
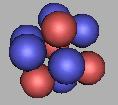 10Be(2) |
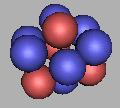 11Be(2) |
|
|
|
我们可以看到,在质子的夹隙填充中子,会使中子太过密集,因此9Be(2)――14Be将是非常不稳定的。
我们可以看到,14Be已经达到中子饱和状态,每一个质子周围都可以达到六个中子。任何方向一个中子临近14Be,都会造成14Be的分解。因此,Be元素的原子核最多排布到14Be。没有比14Be更重的Be原子核。
(二)原子核所形成的化学属性
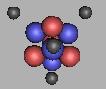 |
如图:8Be原子核中的质子的分布,四个质子位于四面体的四个顶角,Be原子的四个电子分布在四面体中心和四个外表面面中心的连线上。质子的对外界电场力的作用都会受到该方向三个电子电场作用的屏蔽。每一个电子都会受到三个质子电场力的作用。因此,Be是一种稳定的原子。不易失去电子,也不易得到电子。 |
5、硼原子核 3D源文件
(一)原子核属性
硼原子核具有5个质子,可能存在的硼原子核为7B、8B、9B、10B、11B、12B、13B、14B、15B、16B、17B,如图:
|
|
|
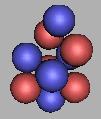 10B |
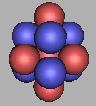 11B |
未曾发现的硼原子核有7B、16B。其中,7B应该是比较容易被发现。因为较为稳定。
其中11B是最为稳定的核结构,那么以此为基础,在相邻的两个质子间进行填充。由于中间的三个质子周围的中子比较密集,那么,比较稳定的力学结构应该是中间的两个质子之间不容易填充,因此先排布两端。那么可以排布到12B、13B、14B、15B、16B、17B。如图:
|
|
|
|
|
|
这样,排布到17B时,质子周围的中子已经非常的密集。这样排布,那么B原子核最多到达17B。
(二)原子核所形成的化学属性
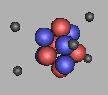 |
在硼元素中,11B最为稳定,我们就以它来分析B原子的化学性质,如图: 11B是由一个三质子环以及在环的两端各分布一个质子所形成,因此它是一个有两个正四面体所合并的六面体。但是,B原子只有5个电子,因此,它不能每一个电子都分布到一个面上,形成一种较为稳定的结构。因此,单质的B原子应该比较容易和别的元素化合。 |
在化合的过程中,由于缺少一个面并且该面是由三个质子对外界提供作用。比较容易形成稳定的化合物。关于鹏在化学反应中反映出正三价,和这个是不是有绝对的关系,尚需要确定。
硼和其它的元素化合后,核外电子的分布必然要改变。
6、碳原子核3D源文件
(一)原子核属性
碳原子核具有6个质子,可能存在的碳原子核为9C、10C、11C、12C、13C、14C、15C、16C、17C、18C、19C、20C。其中未曾发现的只有20C,20C为不能发现的原子核。碳原子核因为包含六个质子,那么在排布结构的选择上较为多一些。可以分为三个质子一环,和四个质子一环。我们先来看三个质子一环的。
(1)三质子环碳原子核结构
第一种,最大作用力方案。
三个质子一环又分两种排布方案,一种方案是最大最用力原则,即:中子先分布到给与中子最大作用力的稳定结构上。如图:在9C上下三个质子各分布一个中子。这样11C则到达一个稳定的结构,并且可以作为一个基本的c核对中子填充,从而得到大于11C的碳核。
|
|
|
在上图中,11C是稳定的结构,这一点和《核素常用数据表》中的是不同的,《核素常用数据表》所列出的11C并不是很稳定,半衰期为20.39秒。因此11C(1)不是《核素常用数据表》所列出的11C。应该还未曾发现。
两个质子间隙去填充中子,如果在两端填充,那么两端的质子数会聚集到四个中子在一起,那么将是非常不稳定的。但可以填充6个中子,也就是填充到17C。如图:
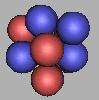 12C(1) |
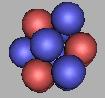 13C(1) |
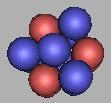 14C(1) |
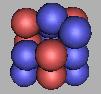 15C(1) |
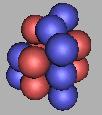 16C(1) |
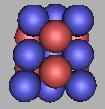 17C(1) |
至于中间还存在两个中子间的空隙,但由于中子太过密集,不能再进行填充了,因为任何一个中子的接近,都可能使17C裂解。如果还可能填充的话,那么在17C的基础上,采用第一种方案最多还可以再填充三个,每两个质子之间填充为一个中子。采用这种方法排布18C到20C,应该是没有意义的。但是,在下一种方法中最后三种C原子核和这里没有意义的三种C原子核是完全相同的。可参见。
第二种、最大可能方案
从原子核俘获中子来看,由于9C原子核中间质子相邻最近,在中间相邻最近两个质子间的填充是成功率最高的。另一方面,在《核素常用数据表》中,12C、13C、14C是稳定的结构,那么传统中所测定的应该不是第一种不方案中的C核,应该是如下的排布。如图:
|
|
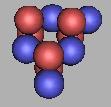 11C(2) |
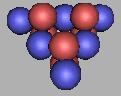 12C(2) |
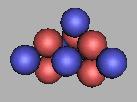 13C(2) |
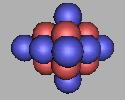 14C(2) |
采用第二种排布方法,从12C到14C都是力学稳定的结合状态,那么可以以14C最为基本的核,进行中子填充。两个相邻质子填充一个中子,那么在14C的基础上,还可以再填充6个中子,也就是碳原子核采用第二种排布方法,核子数最多为20个,质量最大为20C。如图:
|
|
|
|
|
|
在第一种排布方案中,排布到17C后为什么不能排布中间的三个中子?这是因为两旁排布完毕之后,再增加核子只会导致原子核的分裂,因此不能增加。但是如果先存在中间的三个中子,而后再排布两旁的,那么和先排布两旁的相比,再排布中间的,原子核本身具有比较好的稳定性。
(2)四质子环碳原子核结构
由于c质子数只有六个,因此组建四质子环结构稳定性不如三质子环。但这并不能表示它不能存在。如图:
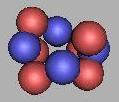 10C(3) |
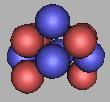 11C(3) |
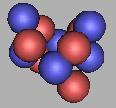 12C(3) |
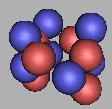 13C(3) |
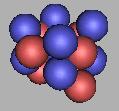 14C(3) |
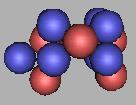 15C(3) |
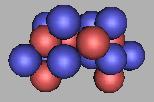 16C(3) |
如上C原子核的排列都是不稳定的,14C、15C、16C可以存在稳定的排布结构,但并未曾发现,如图:
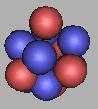 14C(4) |
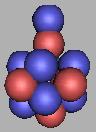 15C(4) |
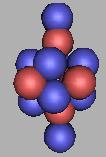 16C(4) |
其中以16C(4)核为基础进行中子填充,在稳定性的基础上可以再填充两个中子,如图:
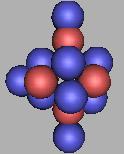 17C(4) |
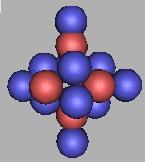 18C(4) |
如上17C(4)、18C(4)是可以被发现的。此外如果采用每两个质子之间填充一个中子的方案,还可以再填充10个中子,也就是说,C原子核的四质子环最大值是28C,不能发现比28C还要重的碳原子核。但由于质子数只有六个,四质子环的稳定性较差,在客观中被发现的可能性并不大,因此这里就不进行填充了。
(二)原子核所形成的化学属性
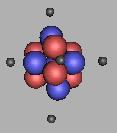 |
虽然自然界中12C的丰度最高,同时也存在其它的可能性的稳定性的C核的存在,在这里我采用11C(1)为例来考察C原子核的化学属性。如图: 11C(1)原子核的质子可以构成5个面,有四个质子构成的面为3个,三个质子构成的面有两个。但是C原子核却有6个电子,多余的这个电子需要在第二个层次上进行排布。因此,C原子核外电子出现第一个两电子层。这是从力学的结构上来构建的核外电子层结构。这和传统观念中的核外电子层是不同的。这里需要注意,一切是以力学的结构作为出发点。我在做这个最后一个电子没有摆放好位置,需要注意。 |
这个电子应该摆放到两个相邻质子中点和某一电子平面的中心连线上。由于作图的困难,后面几个原子就不再做核外电子分布图乐,而仅进行介绍一下。这个电子不需要多大的作用就可以在各个平面之间跳跃转换,因此,是对光的强吸收材料。碳和石墨都是黑色的,和这个核外电子层的结构不无关系。
由于原子核中的质子对核外电子的作用都较强,三个质子和四个质子组成的平面,并且最外层电子只有一个。因此,碳可以获得电子。
7、氮原子核3D源文件
(一)原子核属性
氮原子核具有7个质子,可能存在的氮原子核为11N、12N、13N、14N、15N、16N、17N、18N、19N、20N、21N、22N、23N、24N。还未曾发现的有11N、22N、23N、24N,其中22N、23N,难以发现。24N不能被发现。
(1)三质子环氮原子核结构
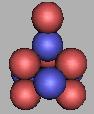 11N |
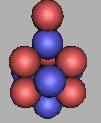 12N |
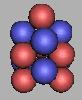 13N |
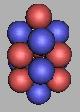 14N |
其中到14N到达最稳定的核结构。在14N中,在两个三质子环之间,三对两个质子并列到一起,如果中子首先填充到这样的两个质子之间,那么将会形成三个较为稳定的N核,其中,15N、16N,应该比较稳定的。以17N为基础,首先在顶端一个质子填充,形成18N,它也是较为稳定的。如图:
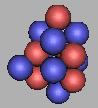 15N |
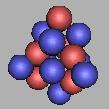 16N |
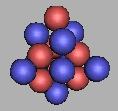 17N |
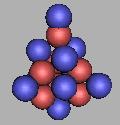 18N |
以18N为基础。在核外两个质子之间填充,可以再填充6个中子,即:N最大质量为24N。如图:
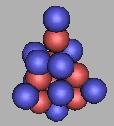 19N |
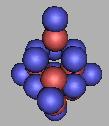 20N |
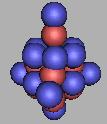 21N |
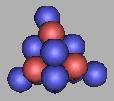 22N |
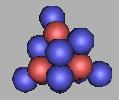 23N |
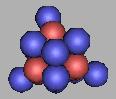 24N |
从19N到24N,都是不稳定原子核。
(2)四质子环氮原子核结构
采用四质子环来构建氮原子核,也是不稳定的,其原因就在于质子数少,不够双层的四质子环,如图:
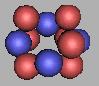 11N(2) |
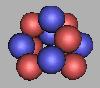 12N(2) |
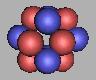 13N(2) |
排列到13N时,已经到达四质子环氮原子核的最稳定结构(由于存在质子中子的不对称分布,仍然是不稳定的),可以在这个基础上进行填充,可以再填充上9个中子。也就是说采用四质子环来构建氮原子核,其质量最大为22N。如图:
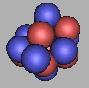 14N(2) |
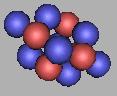 15N(2) |
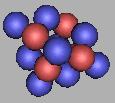 16N(2) |
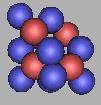 17N(2) |
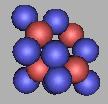 18N(2) |
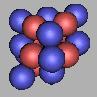 19N(2) |
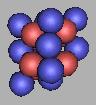 20N(2) |
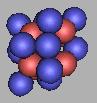 21N(2) |
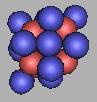 22N(2) |
(二)原子核所形成的化学属性
14N原子核中的质子构成七个平面,7个电子可以分布在各个的平面上。其中,四个质子构成的面为3个,三个质子构成的面为四个。但是,顶端的一个质子构成三个质子平面,这三个平面和四个质子构成的平面在对电子的束缚力上会存在不同。
8、氧原子核3D源文件
(一)原子核属性
氧原子核具有8个质子,可能存在的氧原子核为12O、13O、14O、15O、16O、17O、18O、19O、20O、21O、22O、23O、24O、25O、26O、27O、28O、29O、30O、31O、32O、33O、34O。未曾发现的氧原子核为12O、23O、25O、26O、27O、28O、29O、30O、31O、32O、33O、34O。其中27O、28O、29O、30O、31O、32O、33O、34O可能是采用任何方法不能实现的原子核。
(1)三质子环氧原子核结构
由于氧具有8个质子,采用三质子环构建,那么氧原子核一定是椭圆体。不符合力学的原则。因此,采用三质子环构建,不是最佳的构建方法。包含8个质子的氧原子核是由三质子环和四质子环过渡的中间点,因此,三质子环氧原子核结构应该还是可以存在的。 如图:
|
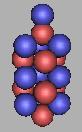 18O(1) |
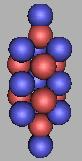 19O(1) |
17O(1)、18O(1)、19O(1)都是较为稳定的原子核,其中17O(1)最为稳定。填充中子可以在这种核上填充,那么在任意两个中子间填充一个中子,可以再填充上15个中子,也就是说最大可以达到34O。但从力学的角度来说,三质子环氧原子核结构本身就很少见了,那么采用大量中子填充的方法,并不是很现实。当然,如果可以得到大量的三质子环氧原子核结构的17O,那么也不是不可能。如图:
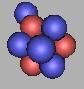 20O(1) |
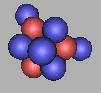 21O(1) |
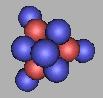 22O(1) |
 23O(1) |
 24O(1) |
 25O(1) |
 26O(1) |
 27O(1) |
 28O(1) |
 29O(1) |
 30O(1) |
 31O(1) |
 32O(1) |
 33O(1) |
 34O(1) |
可以肯定,20O(1)到34O(1)都是不稳定的。由于中子高度密集。后面的几乎没有存在的可能性。三质子环氧原子核结构,考虑到中子之间的排斥力,应该最多排布到25O,当然不能是上面的排布顺序。在上面的图中,任何两个质子之间的空隙都给填充了。填补的6个中子应该均匀的分布到质子之间的空隙中才行。考虑到三质子环的稳定性较好,也给画上了。
(2)四质子环氧原子核结构
采用四质子环来构建氧原子核结构,和《核素常用数据表》中的氧的稳定性是相吻合的。如图:
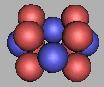 12O |
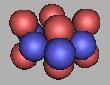 13O |
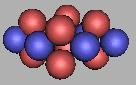 14O |
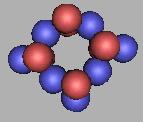 15O |
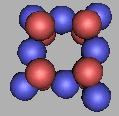 16O |
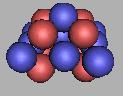 17O(2) |
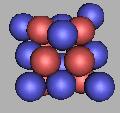 18O(2) |
在16O时,达到稳定氧原子核结构,17O(1)和18O(1)也是稳定的氧原子核,其中18O(1)最为稳定。 在排布中,12O之后也可以按最大最用力原则去排布13O到18O,其中18O(1)是相同的。如图:
.jpg) 13O(2) |
.jpg) 14O(2) |
.jpg) 15O(2) |
.jpg) 16O(2) |
.jpg) 17O(3) |
采用这样的排布方法,在原子核的稳定性上是不同的。应该存在稳定的14O(2),15O(2)、16O(2)、17O(1)也是较为稳定。18O(1)最为稳定。两种不同的排列,原子核的属性,比如放射性、半衰期,力学结构的不同,其属性也必然是不同的。
在18O(1)基础上填充中子,可以再填充8个中子。也就是说,四质子环氧原子核结构最大质量为26O(2)。如图:
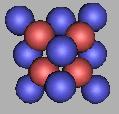 19O(2) |
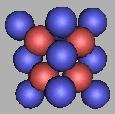 20O(2) |
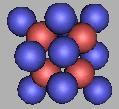 21O(2) |
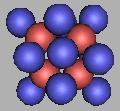 22O(2) |
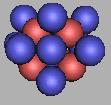 23O(2) |
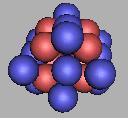 24O(2) |
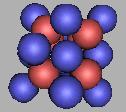 25O(2) |
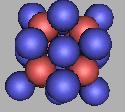 26O(2) |
(二)原子核所形成的化学属性
氧原子核中包含有8个质子,形成以质子为顶角的正立方体。那么氧原子核具有6个面。分别可以排布六个电子。并且六个方向各向同性。余下的两个电子必须排布在第二层。
9、氟原子核3D源文件
(一)原子核属性
氟原子核具有9个质子,由于质子的数量已经可以组建两个四质子环,因此,氟原子核三质子环应该是不能存在的。另一方面,不能组建两个5质子环,采用5质子环的稳定性太差,氟核容易分解或者转化成四质子环。因此,这里采用4质子环来组建。如图:
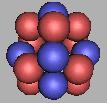 15F |
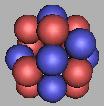 16F |
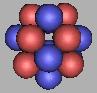 17F |
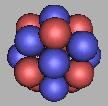 18F |
从排布结构上,18F到达氟原子核最稳定的结构。这一点和《核素常用数据表》,《核素常用数据表》的数据表明19F最为稳定。从排布上看,再增加一个中子,只能造成氟原子核不稳定。因此,我怀疑,《核素常用数据表》的数据是不是存在问题。从质子和中子的排布上来看是不可能的。18F应该最为稳定(19F也是稳定的,但不如18F更为稳定)。以18F为基础对中子进行填充,可能存在的填充可以再填充九个,这9个应该是可以被发现的。
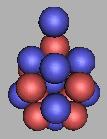 19F |
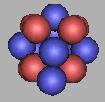 20F |
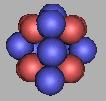 21F |
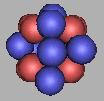 22F |
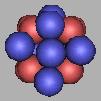 23F |
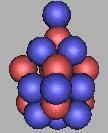 24F |
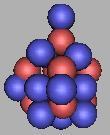 25F |
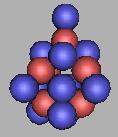 26F |
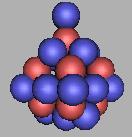 27F |
如果每两个相邻质子之间都填充一个中子的话,那么在27F之后还可以再填充8个,也就是说,可以填充到35F。但这样,中子已经太过密集了。一个质子和六个中子结合,在17B中存在并且被发现。其中一个质子可以和六个中子结合。我想,一方面在于三质子环较为稳定,另一方面说明,在确定的体积里中子的含量较小,那么在三质子环中,是可以存在少量的一个质子和六个中子结合的形式。但是,随着质子数量的增加,中子的数量也在大幅的增加,采用一个质子和六个中子结合的形式,在已经发现的原子核中极为罕见。那么这说明,中子之间存在斥力。一个质子和多个中子结合存在确定的关系,它和原子核体积中中子的平均密度也存在一定的关系,并不是单方面的。
由于《核素常用数据表》所列的数据最大为25F,所以28F到35F我就不画了。35F是从排列与组合上的最大F原子核。但28F到35F不容易实现,也不容易发现。
(二)原子核所形成的化学属性
氟原子核具有9个质子,采用四质子环来组建。氟原子核具有9个面,其中有四个质子构成的面为5个,三个质子构成的面为4个。
10、氖原子核3D源文件
(一)原子核属性
氖原子核具有10个质子,可以组建4质子环和5质子环。
(1)四质子环
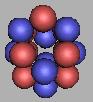 18Ne |
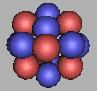 19Ne |
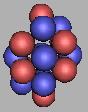 20Ne |
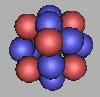 21Ne |
 22Ne |
22Ne达到最为稳定的结构,20Ne、21Ne也具有稳定性。以22Ne为基础填充,可以再填充6个中子,也就是说,Ne的四质子环原子核结构可以达到28Ne。如图:
 23Ne |
 24Ne |
 25Ne |
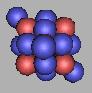 26Ne |
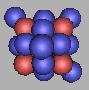 27Ne |
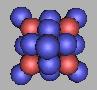 28Ne |
(2)五质子环
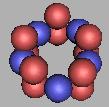 15Ne |
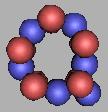 16Ne |
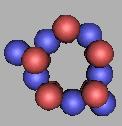 17Ne |
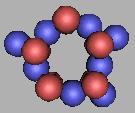 18Ne(1) |
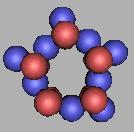 19Ne(1) |
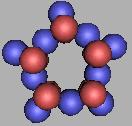 20Ne(1) |
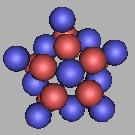 21Ne(1) |
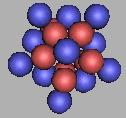 22Ne(1) |
20Ne达到稳定状态,21Ne、22Ne也是稳定状态。在稳定性的原子上,和四质子环是相似的。以22Ne为基础填充中子,可以再填充10个,也是就说Ne原子核可以最大达到32Ne。如图:
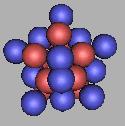 23Ne(1) |
 24Ne(1) |
 25Ne(1) |
 26Ne(1) |
 27Ne(1) |
 28Ne(1) |
 29Ne(1) |
 30Ne(1) |
 31Ne(1) |
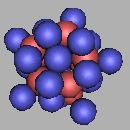 32Ne(1) |
随着中子的增加,核的稳定性越差,其中27Ne、28Ne为难发现原子核,29Ne、30Ne、31Ne、32Ne为不能发现原子核,任何一个外界核子触动28Ne(1),都可能造成核反应。
关于五质子环的排布,从23Ne(1)到32Ne(1),我这里排布的顺序不是按照核的稳定性来排布的,而是为了方便。这样的排布存在一点问题,不能采用这样的依次排列,应该采用在两个质子之间填充的中子进行均分的方法。就是把中子平均的分配到球面上。
(二)原子核所形成的化学属性
四质子环的Ne原子,具有12个面,也就是说,在增加两个电子也是稳定的。因此,Ne有可能参加化学反应。这一点和传统的惰性气体的看法是不同的。
五质子环的Ne原子,最接近原子核的两个电子的电离能特别高,可根据这点来判断是不是五质子环。
此外,五质子环的Ne原子核的电场是近乎椭球形,我的数学不好,对此不能有什么结论。
七、重原子核质子环的封闭问题
采用球壳式原子模型来构造原子核,由于中子和质子都是确定的大小,因此,在质子环的封闭上就存在一个问题,我们可以看到,采用五质子环在封闭环口的时候就出现五个质子口的问题。那么10质子环11质子环就是不可想象的了。
我想这一点可以采用缩减质子环的方法来实现,比如一个11质子环,不能一次封闭缺口,而是逐次递减,可以采用6中子环,而后再3质子环,最后再一个中子收口。
后语:关于原子核观念的思考大概从00年冬天写过一篇电的属性的文章后开始的,最初感觉采用作用力的模式来探索原子核是非常的困难。从传统的观念中很难得到启发性的东西。因为都是采用数理的模式。最后屏弃所有书本上的内容,对原子核的组成进行力学分析和尝试而得出的这样的看法。
如果原子核完全依赖于力学的模式,那么这决定原子的结构也完全依赖于力学的模式。这样一条思路从逻辑上似乎没有什么问题。最初采用纯想象的模式来判断原子核的可能性的力学结构。但实在是进展缓慢。后来采用了3dmax,呵呵,比单纯的想象要好得多。去年冬天才开始建模,到今年四月份1到22号元素完成原子核可能性的核模型,23号元素还没有完成。大概有上千个吧。对于元素的稳定性核,基本上吻合。可惜的很,我的硬盘报废了。那些东西全没了。
这是一个工作量很大的工作。我把这些方法给公布出来,希望利于有志于此的朋友探索。
这个理论模型并不是完美的,还存在困难,比如元素周期律、放射性的量值和计算。对于原子核来说,这仅仅是一种新思路的开端。
本文3d模型的源文件是采用3dmax3.1做的,低版本的不能打开。我把它分开放置在本文每一号元素的标题上,总计大小为2.01MB,由于一个网站不支持,所以分开打包。
于2002年9月11日上午6点
![]() 版权所有,保留一切权力,未经授权使用将追究法律责任 版权说明 © Copyright Authors
版权所有,保留一切权力,未经授权使用将追究法律责任 版权说明 © Copyright Authors
物理科学探疑